泉源 :华尔街见闻
美国FDA答应 为礼来以Kisunla为商品名donanemab在美国出售该药扫清停滞 ,它将成为在美上市第二种的减缓脑萎缩疾病药物。其美国竞品Leqembi的开辟 商渤健盘中一度跌近3%。
美国医药巨头礼来治疗阿尔兹海默症的新药扫清了在美上市的停滞 ,股价盘中大幅收窄跌幅。
美东时间7月2日周二美股午盘,早盘革新 日低时跌逾3.9%的礼来(Eli Lilly Co.)加快 反弹,日内跌幅收窄到1%以内,一度仅跌0.26%。
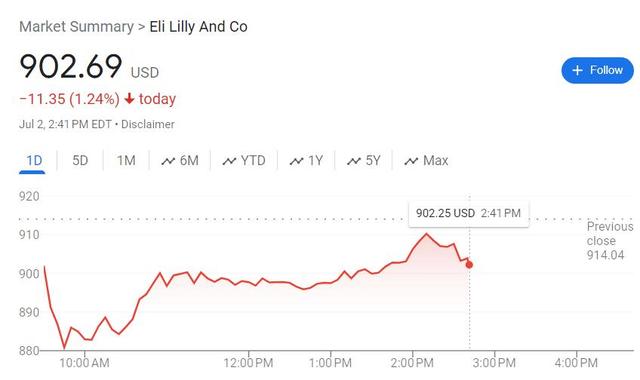
周二午盘时段,美国羁系 机构食药监局(FDA)正式答应 礼来的新药donanemab用于治疗早期阿尔茨海默症(AD)的成年患者。获批意味着,礼来能以Kisunla为商品名donanemab在美国出售这款新药,它将成为在美上市的第二种获批治疗减缓脑萎缩疾病药物。
本次FDA答应 基于一项大规模的三期双盲安慰剂对照试验。试验收录了1736 名早期 AD 患者,他们每附近 担当 一次 donanemab、即Kisunla注射或安慰剂治疗,最长治疗时间72周。试验重要 结果 是综合AD评分量表 (iADRS) 评分的最小二乘均值 (LSM) 变革 ,分数越低表现 侵害 越严峻 。在低/中相干 病理卵白 tau 人群中,到76 周时,担当 Kisunla治疗者的iADRS 评分相对于基线的 LSM 变革 为 -6.02,在安慰剂组中则为-9.27。
Kisunla是一种每附近 注射一次、一次剂量350 mg/20 mL 的单克隆抗体静脉注射剂,实用 于有轻度认知停滞 (MCI) 患者以及进入轻度痴呆阶段、已确认脑中存在病理分子淀粉样卵白 的AD患者。礼来对Kisunla订价 为每瓶 695.65 美元,12个月的治疗费用为3.2万美元。
有业内媒体指出,Kisunla环球 首个也是唯逐一 个有证据支持当大脑中淀粉样斑块被打扫 时克制 治疗的淀粉样卵白 靶向治疗药物。这一证据支持结论可以低落 治疗本钱 ,并镌汰 药物注射次数。
有媒体批评 称,Kisunla获批对礼来及其投资者来说是巨大的胜利,三年多前,这种药物在临床试验中表现 了治疗AD的远景 ,以后 投资者不停 热切等待 它上市,羁系 方这期间曾多次耽误 答应 。获批还标记 着,市面上有了第二种可减缓600万美国人脑部疾病发病的药物。
Kisunla此次获批不算不测 。三周前的6月10日,FDA的专家委员会就以11票全票同意 承认 该药物的有效 性,对于ARIA副作用等题目 ,同样11票同意 认定该药物对病患利大于弊,获益大于风险。疗效数据如下,治疗76周iADRS延缓降落 22%,CDR-SB评分延缓降落 29%。
当时 媒体指出,Kisunla获批后,将直接同卫材(Eisai Co.)/渤健(Biogen)连合 开辟 的客岁 初在美国上市药物Leqembi 竞争。Leqembi 也实用 于早期AD患者,即存在轻度认知停滞 或处于轻度痴呆状态的AD患者。
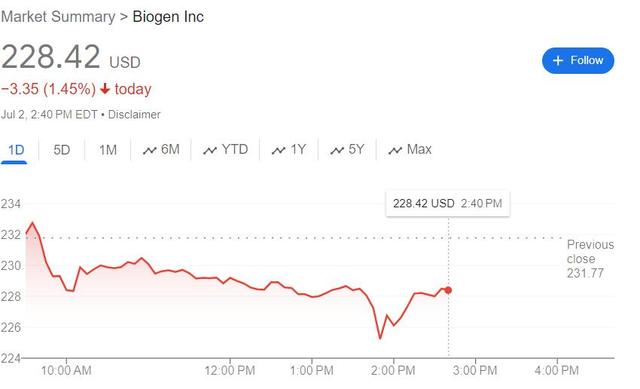
本周二Kisunla获批后礼来盘中收窄跌幅的同时,渤健午盘革新 日低,日内跌幅扩大到近2.9%。





0 评论